Medisch nieuws
Autologe hematopoietische stamceltransplantatie in MS
De voorbije 20 jaar werd sporadisch autologe hematopoietische stamceltransplantatie gebruikt bij de behandeling van ernstige vormen van MS. Recent kwam de behandeling opnieuw onder de aandacht. Een uitzending op Koppen riep heel wat vragen op bij patiënten. We gaan hieronder dan ook graag in op een recente publicatie waarin een stand van zaken wordt gemaakt na 20 jaar ervaring met deze behandeling.
Inleiding
Hematopoietische stamceltransplantatie wordt klassiek gebruikt bij de behandeling van bloedkankers. De bedoeling is dan de vernietiging van de kankercellen door hoge dosissen chemotherapie, waarna het immuunstelsel hersteld wordt door een autologe of een allogene stamceltransplantatie. Bij een allogene transplantatie verschillen de donor en de receptor immunologisch en kunnen de getransplanteerde stamcellen aanleiding geven tot een nieuw immuunsysteem en de na de chemotherapie eventueel nog overblijvende kankercellen vernietigen. Deze gunstige bijwerking, waarbij overblijvende tumorcellen worden vernietigd, is de graft-versus-tumor reactie. Helaas kunnen de getransplanteerde cellen zich ook richten op de eigen cellen van de receptor, zodat reacties ontstaan die zelfs tot de dood kunnen leiden. Men noemt dit de graft-versus-host ziekte. Omwille van het mogelijke optreden van deze graft-versus-host ziekte gebruikt men in auto-immune aandoeningen zoals MS liever de autologe hematopoietische stamceltransplantatie, waarbij eigen stamcellen worden getransplanteerd die dan wel het immuunsysteem vernieuwen of resetten, maar niet leiden tot de soms levensbedreigende graft-versus-host ziekte.
Procedure
Er zijn veel verschillende protocols gebruikt, zowel wat betreft de voorbereiding van de transplantatie (chemotherapie) als bij de transplantatie zelf. Ook blijft het totaal aantal behandelde patiënten eerder beperkt. We proberen hieronder dan ook vooral te spreken over de voor- en nadelen die in de verschillende behandelingsschema's terugkwamen.
Resultaten op klinische evolutie
Alle gepubliceerde fase I/II studies tonen dat autologe hematopoietische stamceltransplantatie leidt tot een stabilisatie, en soms een verbetering van de ziekte, althans op middenlange termijn. Een retrospectieve analyse van de Europese Groep voor Blood- en Mergtransplantatie (EBMT) toont dat na 3 jaar 74% en na 5 jaar 45% van de patiënten stabiel gebleven is. Ongeveer de helft van de behandelde personen zou een verbetering kennen van de EDSS, een maat voor functionele weerslag van de ziekte. Op opflakkeringen is er een uitgesproken effect, met een nagenoeg volledige aanvalscontrole de eerste jaren na de therapie.
Resultaten op radiologische evolutie
In de meeste studies was er een belangrijk effect op het aantal contrastcapterende lesies, en op het verschijnen van nieuwe lesies. Daarentegen werd geen invloed gezien van de behandeling op het ontstaan van hersenatrofie of het geleidelijk afnemen van het hersenvolume naarmate de ziekte vordert.
Veiligheid
De transplantatie gerelateerde mortaliteit, dus de kans om door complicaties van deze procedure te overlijden is vandaag de dag 1-2%. In de periode 1995-2000 was dit nog 7.3%. Deze daling van sterfterisico houdt waarschijnlijk verband met aanpassingen van de protocols, een betere patiëntenselectie, en de toegenomen ervaring van hematologen en neurologen.
Andere frequente gevolgen van de behandeling zijn koorts door gebrek aan witte bloedcellen,, infecties, diarree. Als laattijdige complicatie kunnen andere autoimmune aandoeningen ontstaan, zoals autoimmuun schildklierlijden. Ook onvruchtbaarheid kan tot stand komen door deze behandeling.
Besluit
Na 20 jaar toepassing is de autologe hematopoietische stamceltransplantatie voor MS geëvolueerd naar een te overwegen behandelingsoptie die echter nog steeds een mortaliteit met zich meebrengt van 1-2% en daarnaast tot ernstige en blijvende bijwerkingen kan aanleiding geven. De behandeling wordt momenteel dan ook gezien als een optie in goed geselecteerde patiënten. Om deze behandeling te overwegen moet er sprake zijn van een beginnende (minder dan 5 jaar sinds ziektebegin, patiënt max. 40 jaar) maar zeer aggressieve MS, waarbij opflakkeringen elkaar blijven opvolgen ondanks ‘klassieke' behandeling. Voor deze patiëntengroep zijn er momenteel ook andere behandelingsopties beschikbaar, zoals Tysabri en Lembrada. De precieze plaats van elk van deze behandelingen is nog onduidelijk, en vergelijkende studies zijn nodig om hier een beter zicht op te krijgen.
Prof. Dr. Bénédicte Dubois
Dienst Neurologie Universitaire Ziekenhuizen Leuven - KU Leuven
Bron:
- D. Curro et al.
Autologous hematopoietic stem cell transplantation in multiple sclerosis: 20 years of experience.
Neurol. Sci. 2016, Apr. 12
De invloed van stress op multiple sclerose
MS is een ontstekingsziekte van het centraal zenuwstelsel met een onvoorspelbaar verloop. Tijdens de eerste jaren van de ziekte maken de meeste personen opflakkeringen door met nieuwe of toegenomen neurologische klachten. De opflakkeringen komen overeen met het optreden van nieuwe ontstekingshaarden ter hoogte van de myeline, zichtbaar op de NMR beelden van hersenen en ruggenmerg. Daarnaast gaan heel wat personen met MS op langere termijn geleidelijk aan achteruit wat overeenkomt met toenemende schade ter hoogte van de zenuwvezels. Dit proces van toenemende schade is niet of slechts zeer laattijdig zichtbaar op de NMR beelden van het centraal zenuwstelsel.Het verloop van MS verschilt van persoon tot persoon. Waarom dit zo is, weten we niet. Wellicht wordt dit bepaald door een combinatie van genetische factoren en omgevingsfactoren.
Stamcellen: remyelinisatie en multiple sclerose
- Definitie van stamcellen: een stamcel wordt gedefinieerd als een cel die in staat is om enerzijds zichzelf te vernieuwen en anderzijds zeer gespecialiseerde celtypes te genereren. Stamcellen die in een zeer vroeg ontwikkelingsstadium worden geïsoleerd, hebben een hoger potentieel om zich tot velerlei verschillende cellen te differentiëren dan cellen die in een later stadium worden afgezonderd. Embryonale stamcellen zijn dus het meest ‘pluripotent', anders gezegd: ze hebben het grootste potentieel om in een celkweek verschillende celtypes te genereren, in het bijzonder zenuwcellen en gliacellen, waaronder oligodendrocyten, die de myelineschedes produceren.
Naast embryonale stamcellen bestaan er ook foetale stamcellen en volwassen stamcellen, die afkomstig zijn uit beenmerg (mesenchymale stamcellen), hematopoïetische stamcellen (voorlopercellen uit het bloed) en neurale stamcellen (afkomstig diep uit de hersenen, nabij de wanden van de ventrikels met hersenvocht).
Technisch is het niet zo eenvoudig om ervoor te zorgen dat die verschillende stamceltypes zich differentiëren tot een goed gedifferentieerde doelcel, bijvoorbeeld tot een zenuwcel of tot een oligodendrocyt. In het centrale zenuwstelsel (hersenen en ruggenmerg) zijn voorts diffuus ‘oligodendrocytvoorlopercellen' aanwezig, die ook kunnen worden beschouwd als specifieke stamcellen voor dit celtype. Deze voorlopercellen kunnen sommige MS-plaques gedeeltelijk, maar toch doeltreffend remyeliniseren. De door deze voorlopercellen opnieuw gevormde myelineschede is doorgaans fijner, dunner en minder lang. Helaas kan de opnieuw aangemaakte myeline zelf weer het doelwit worden van het vernietigingsproces en dus worden vernietigd. - Neurobescherming bij multiple sclerose: het betreft hier een belangrijke therapeutische doelstelling die door onze huidige therapieën nog niet wordt vervuld. Deze neurobescherming heeft twee componenten: 1) preventie van verlies van zenuwvezels, axonen genoemd, die ofwel kunnen verloren gaan door transsectie tijdens de acute ontsteking, ofwel chronisch, gedurende maanden en jaren, als gevolg van het verloren gaan van hun beschermende myelineschede; 2) het bevorderen van remyelinisatie op plaatsen waar de myelineschede is vernietigd. Deze twee fenomenen hangen samen, want uiteraard is het onmogelijk om axonen te remyeliniseren als die al aan het degenereren zijn. We hebben goede redenen om aan te nemen dat de progressieve ziektefase, die gemiddeld 10 tot 15 jaar na de eerste aanval wordt waargenomen, rechtstreeks samenhangt met deze axondegeneratie. 15% van de MS-patiënten maken bovendien geen relapsing-remittingfase door, maar treden meteen in een progressieve fase van axondegeneratie.
- Stamceltherapie bij multiple sclerose: we kunnen ons twee mechanismen voorstellen, die elkaar overigens niet uitsluiten: ofwel vervanging van de stamcellen, in het bijzonder de oligodendrocytvoorlopercellen, door cellen uit een externe bron die bij de patiënt worden ingespoten; ofwel verhoging van het endogene herstel door gebruik te maken van eigen stamcellen van de betrokkene en in het bijzonder door de oligodendrocytvoorlopercellen te stimuleren.
a) Celherstel door exogene cellen schept tal van problemen. De stamcellen moet zich differentiëren tot een aanzienlijke hoeveelheid van het gewenste celtype, bijvoorbeeld oligodendrocytvoorlopercellen, de differentiatie moet stabiel zijn, er mag geen overmatige celproductie zijn die tot een tumor evolueert, en ten slotte moeten de stamcellen zich naar de pathologische zone begeven. We weten evenwel dat stamcellen van nature worden aangetrokken door pathologische zones die herstel vergen. Deze eigenschap heet ‘pathotropisme'.
b) Het bevorderen van mechanismen van endogeen herstel: deze aanpak is in de nabije toekomst wellicht realistischer en haalbaarder. We weten dat er in MS-plaques vaak oligodendrocytvoorlopercellen aanwezig zijn, die echter door de inflammatoire omgeving geremd lijken te worden, wat de remyelinisatie verhindert. Tegenwoordig wordt in tal van studies geprobeerd een helderder licht te werpen op de pro- en antiremyelinisatiemechanismen en op de moleculen die de remyelinisatie bevorderen of afremmen. Zo is er een molecule, lingo genoemd, dat in experimentele modellen het doelwit vormt van een monoklonaal antilichaam tegen lingo, met als gevolg dat de remyelinisatie wordt bevorderd. De eerste klinische tests op mensen zijn van start gegaan in het kader van oogzenuwontsteking als eerste symptoom van multiple sclerose. Doel is te weten of dit antilichaam tegen lingo kan helpen om de oogzenuw te beschermen, degeneratie van de zenuwvezels te beletten en aldus een scherper zicht te behouden.
Zo is er nog een andere haalbaarheidsstudie uitgevoerd met mesenchymale cellen die bij de patiënten zelf zijn gehaald om progressieve secundaire vormen van multiple sclerose te behandelen. De initiële resultaten waren bemoedigend voor de gezichtsfunctie.
Conclusie: het onderzoek van stamcellen ter behandeling van multiple sclerose zal ons beslist kostbare aanwijzingen geven over de ziektemechanismen en de cruciale kwestie van de neurobescherming.
De ethische problemen (gebruik van embryonale of foetale stamcellen) en technische problemen blijven echter bijzonder groot. Stamcellen die bij de patiënt zelf worden gehaald, scheppen geen ethische problemen en worden niet vernietigd door het immuunsysteem van de betrokkene, maar hebben een lager potentieel om zich tot het gewenste celtype te differentiëren. Zelfs in de hersenen van een volwassene zijn er voorlopercellen die nog altijd in staat zijn om zich te differentiëren en andere, door een ziekteproces vernietigde cellen te vervangen.
Professor Christian SINDIC
Juli 2013
Neuromyelitis optica: een variant van MS?
Neuromyelitis optica (NMO of ziekte van Devic) is een ontstekingsziekte die vooral de oogzenuwen en het ruggenmerg treft. Andere kenmerken zijn het meer voorkomen bij vrouwen dan bij mannen, de aanwezigheid van langgerekte ruggenmergontstekingen bij beeldvorming, en de afwezigheid van oligoclonale bandjes in het cerebrospinaal vocht. Sommige elementen lijken dus op MS, andere verschillen ervan, en het is lang onduidelijk geweest of en welk verband er precies bestaat met MS. Onderzoek liet echter toe een eiwit te identificeren dat kenmerkend is voor NMO: de aquaporine-4 antilichamen. Nochtans vindt men dit eiwit ook bij sommige personen die herhaaldelijk een oogzenuwontsteking of een ruggenmergontsteking doormaken, en dus niet de combinatie van beide. Er is daarom sprake van een spectrum van NMO-aandoeningen die onderling verwant zijn, lijken op MS, maar bij nader inzicht verschillen van MS. In dit artikel wordt ingegaan op enkele belangrijke aspecten van NMO-aandoeningen.
Algemeen voorkomen
NMO ontstaat meestal in de vierde levensdecade, alhoewel een eerste opflakkering op elke leeftijd mogelijk is. NMO komt meer voor bij vrouwen dan bij mannen. 3% van de personen met NMO heeft nog een familielid met NMO, wat doet vermoeden dat er voor deze aandoening geen erfelijke oorzaak, maar wel een erfelijke vatbaarheid bestaat. Meer is hierover voorlopig echter niet geweten.
Klinische kenmerken
De meeste patiënten hebben een ziekteverloop dat gekenmerkt wordt door opflakkeringen. Deze aanvallen zijn meestal ernstiger dan bij MS, en betreffen een verminderd zicht (door de oogzenuwontsteking) en gevoels- en krachtsverlies in de ledematen, alsook blaasproblemen (door de ruggenmergontsteking). Een secundair progressief verloop, waarbij klachten dus ook zonder opflakkeringen geleidelijk toenemen komt in NMO zelden voor, in tegenstelling tot MS. Vermoeidheid is zowel bij MS als bij NMO een vaak voorkomende klacht.
Radiologische kenmerken
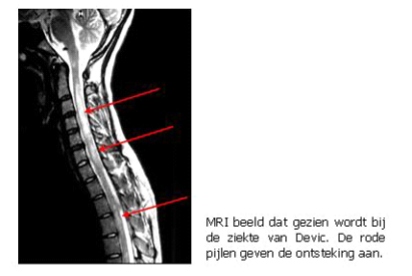
Waar een magnetische resonantiescan (MR) van de hersenen in MS meestal duidelijk meerdere wittestofletsels toont, is dit in NMO veel minder het geval. De MR hersenen kan zelfs normaal zijn. De MR wervelzuil daarentegen toont vaak erg lange ontstekingsletsels.
Bloedtest
Zoals blijkt uit de hoger vermelde kenmerken, is het onderscheid tussen MS en een aandoening van het NMO-spectrum niet altijd evident. Gelukkig leidde wetenschappelijk onderzoek in 2004 dan ook tot de identificatie van de aquaporine-4 antilichamen, die gevonden worden bij personen met NMO, en niet bij deze met klassieke MS. Ook komen bij NMO vaker andere auto-immuunaandoeningen voor zoals auto-immuun schildklierlijden, lupus, myasthenia gravis, e.a. Ook in het bloed vinden we bij NMO meer auto-antilichamen, ook zonder bijhorende auto-immuunziekte.
Behandeling
Zoals bij MS bestaat de behandeling van NMO uit verschillende deelbehandelingen: de behandeling van een opflakkering, de preventie van aanvallen, de aanpak van de symptomen, en de revalidatie. Beide laatste verschillen niet van de behandeling van MS.
Bij het optreden van een acute opflakkering worden baxters cortisone toegediend, zoals bij MS. Vaker wordt daarna wel gedurende enige tijd de cortisone verder gegeven in pilvorm. Indien de aanval hieronder niet verbetert, wordt er overgegaan tot plasmaferese, waarbij de schadelijke stoffen, zoals de aquaporine-4-antilichamen, uit het bloed worden gewassen.
De preventie van opflakkeringen is specialistisch. Belangrijk is wel dat een behandeling voor MS, zoals interferon-bèta of glatirameer acetaat, hier geen goede keuze is.
Besluit
Het is duidelijk dat er vooral voor wat betreft de symptomen, het verloop in opflakkeringen, en de behandeling van deze aanvallen zeker gelijkenissen zijn tussen MS en NMO. Dat verklaart meteen ook waarom deze aandoening aan bod komt in een site voor personen met MS. Toch zijn er wezenlijke verschillen tussen beide ziekten die zich uiten in de verschillende kenmerken op beeldvorming, de aanwezigheid van aquaporine-4-antilichamen in NMO, en een verschillende onderhoudsbehandeling.
Prof. dr. B. DUBOIS
Dienst Neurologie Universitaire Ziekenhuizen Leuven - KU Leuven
April 2013
Bron
JACOB, A., et al., Current concepts of neuromyelitis optica (NMO) and NMO spectrum disorders,
Journal of Neurology, Neurosurgery and Psychiatry 2012, in druk.
Neuromyelitis optica (Neuromyelitis Optica Spectrum Disorder: NMOSD) is een demyeliniserende ontstekingsziekte van het centrale zenuwstelsel die duidelijk verschilt van multiple sclerose (MS). De twee aandoeningen vertonen echter historische overeenkomsten en hebben gemeenschappelijke dysimmunitaire mechanismen.
In westerse landen is NMOSD een zeldzame ziekte. De aandoening komt vaker voor in Azië (Japan). Op basis van de huidige epidemiologische gegevens stellen we vast dat de incidentie van NMOSD bij MS-patiënten 1 % bedraagt (d.w.z. ongeveer 150 patiënten in België). Jarenlang werd de ziekte beschouwd als een speciale vorm van MS, die verantwoordelijk was voor preferentiële aantasting van de oogzenuwen en het ruggenmerg. De functionele prognose was vrij somber, met patiënten die snel ernstige visuele en motorische stoornissen vertoonden binnen vijf jaar na de eerste symptomen. Oorspronkelijk werd de aandoening de ziekte van Devic genoemd en ze werd lange tijd behandeld als MS. Anders dan bij MS is de handicap bij patiënten met NMOSD het gevolg van opflakkeringen die zeer acuut kunnen zijn. Er zijn geen progressieve vormen van NMOSD.
De vooruitgang op het gebied van MRI en immunologie heeft de context van de aandoening volledig veranderd. Dankzij MRI kunnen laesies worden opgespoord die afwijken van de oorspronkelijk beschreven vormen (supratentoriale hersenschade, schade aan de hersenstam en het periaqueductale grijs).
In 2004 toonde een belangrijke publicatie de aanwezigheid aan van specifieke antilichamen die gericht zijn tegen een waterkanaal (AQP4Ab) dat zich op het membraan van astrocyten bevindt. Astrocyten zijn cellen van het centrale zenuwstelsel (CZS) die van wezenlijk belang zijn voor de werking van de neuronen. Ze zijn een soort ‘functionele brug’ tussen de bloedvaten en andere cellen (neuronen en oligodendrocyten). AQP4-antilichamen zijn IgG1-moleculen die worden geproduceerd door immuuncellen (plasmacellen afgeleid van B-lymfocyten). Ze zijn aanwezig bij ongeveer 80 % van de volwassen patiënten die aan NMOSD lijden. De activering van deze B-lymfocyten en hun evolutie tot plasmacellen die AQP4Ab’s synthetiseren, hangen af van stimulatie door T-lymfocyten van de Th17-familie (T helper). Antilichamen worden aangemaakt in het perifere bloed en dringen door de bloed-hersenbarrière. Ze hechten zich vast aan de voetjes van de astrocyten (verlengde van een astrocyt dat naar de capillaire bloedvaten reikt). Hierdoor wordt het complementsysteem geactiveerd. Dit systeem bestaat uit een groep moleculen die een rol spelen in de ontstekingsreactie en de toxische gevolgen ervan voor de cellen. De ontstekingsreactie is bijgevolg gekoppeld aan de activering van complement (CDC) en antilichamen (ADCC). Er ontstaat oedeem in de astrocyten en er treedt een breuk op in de bloed-hersenbarrière. De problematische toestand van de astrocyten veroorzaakt disfunctie van neuronen en oligodendrocyten. Alle verschijnselen samen werken de massale aanmaak van andere witte bloedcellen in de hand (polynucleaire neutrofielen en eosinofielen), wat leidt tot een uiterst significante ontsteking van het weefsel. De neuronen komen al snel onder grote cellulaire druk te staan, functioneren niet meer en sterven af. Deze ontstekingscascade komt heel snel tot stand en resulteert in de symptomen die de patiënt ervaart. De pathogene (ziekteverwekkende) rol van AQP4Ab’s werd aangetoond door NMOSD te triggeren bij proefdieren die serum kregen van getroffen patiënten.
Er werd nog een ander antilichaam, gericht tegen een myeline-eiwit (MOG), in verband gebracht met NMOSD. De precieze rol ervan is minder duidelijk. Het komt slechts voor bij 4 tot 11 % van de patiënten met dit ziektebeeld, vaker bij jongere mensen en zelfs bij kinderen. De persistentie van deze MOG-antilichamen is al een reden op zich om een gerichte behandeling op te starten. Microscopische analyses van het aangetaste weefsel lieten omkeerbare myelineafwijkingen zien, zonder complementactivering of significante inflammatoire infiltratie.
Tot slot worden in 14 tot 22 % van de NMOSD-gevallen geen AQP4- of MOG-antilichamen gevonden en zijn de diagnostische criteria voor deze ziekte vrij streng.
De criteria werden in 2015 verduidelijkt en gepubliceerd. Dit had belangrijke gevolgen voor de therapeutische behandeling van de patiënten. Al bij één typische manifestatie van de ziekte kan op basis van de aanwezigheid van een AQP4Ab in het bloed de diagnose worden gesteld. Zo kan er een doeltreffende onderhoudsbehandeling worden gestart om recidieven te voorkomen. Recidieven kunnen ernstig zijn en worden geassocieerd met een aanzienlijke resterende handicap. Een vroege behandeling van de patiënt is daarom fundamenteel.
De therapeutische strategie
Acute opflakkeringen van NMOSD
Opflakkeringen kunnen een ernstige handicap zijn en een vroege behandeling van recidieven is van wezenlijk belang. Gewoonlijk bestaat de eerste fase van de behandeling van een opflakkering in de intraveneuze toediening van een hoge dosis cortisone, zoals bij multiple sclerose. De patiënt krijgt gedurende 3 tot 5 opeenvolgende dagen intraveneus 1000 mg Solumedrol per dag toegediend. De tijd tot behandeling moet zo kort mogelijk zijn, i.e. zodra de terugval wordt vastgesteld. Het klinische beeld wijzigt doorgaans snel tijdens de behandeling. Als er na enkele dagen geen significante verbetering optreedt, wordt plasma-uitwisseling (PLEX of plasmaferese) aanbevolen. PLEX is een techniek die abnormale antilichamen uit het bloed haalt door middel van een filtratie die sterk lijkt op wat tijdens dialyse wordt gedaan. Dit houdt in dat er een centrale veneuze katheter van groot kaliber moet worden geplaatst, althans tijdelijk. De patiënt wordt vervolgens aangesloten op een machine die het bloed filtert. Het bloed gaat door een membraan dat de antilichamen vasthoudt. Vervolgens wordt het opnieuw bij de patiënt geïnjecteerd. PLEX wordt meestal uitgevoerd in 5 tot 7 sessies over een periode van 2 weken. Anders dan bij MS moet de behandeling met corticosteroïden en/of PLEX worden gevolgd door enkele weken orale toediening van corticosteroïden. Sommige auteurs bevelen zelfs een sterk immunosuppressivum aan in de periode onmiddellijk na PLEX, om reboundverschijnselen te voorkomen. Tot nu toe zijn er geen wetenschappelijke gegevens om de respons op een behandeling met corticosteroïden of PLEX te voorspellen, met name in verband met de aanwezigheid van anti-AQP4Ab. Sommige observationele studies lijken aan te tonen dat patiënten met NMOSD geassocieerd met MOG-antilichamen bijzonder goed reageren op corticosteroïden. Het risico op rebound bij stopzetting van de behandeling is echter relatief hoog.
‘Klassieke’ onderhoudsbehandelingen
Rituximab
Rituximab is een chimeer cytotoxisch monoklonaal antilichaam gericht tegen de CD20-receptor. Een monoklonaal antilichaam wordt aangemaakt door cellen die systematisch hetzelfde molecuul synthetiseren. Het herkent zijn doelwit met perfecte precisie. Wanneer het antilichaam zich aan zijn receptor bindt, veroorzaakt het een opeenvolging van gebeurtenissen die de cel zullen vernietigen. Het geneesmiddel werd oorspronkelijk ontwikkeld en goedgekeurd voor de behandeling van lymfatische tumoren (lymfomen). De cellen met CD-merker CD20 zijn voornamelijk B-lymfocyten. Een klein aantal T-lymfocyten draagt ook deze merker. De term ‘chimeer’ betekent dat een deel van het antilichaam sequenties van aminozuren bevat die afkomstig zijn van muizen. Na infusie van dit monoklonale antilichaam blijft het molecuul 120 uur tot 6 maanden in het lichaam aanwezig. Er worden verschillende doseringsschema's aanbevolen, maar de meeste centra gebruiken een aanvangsdosis van 1 g die na 2 weken wordt herhaald of wekelijks 375 mg/m2 gedurende 4 weken. Het geneesmiddel heeft alle B-lymfocyten na ongeveer 1 maand vernietigd. Er moet echter worden opgemerkt dat slechts een heel klein deel (1 %) van het middel door de bloed-hersenbarrière gaat en het hersenvocht binnendringt. De werkzaamheid van Rituximab werd niet onderzocht in internationale standaardonderzoeken. De huidige gegevens zijn gebaseerd op gepubliceerde reeksen en post-hocanalyses. Het gunstige effect van het geneesmiddel is significant: 80 % verminderde frequentie van opflakkeringen, vooral bij AQP4Ab-positieve NMOSD-patiënten. Mede dankzij een gunstig veiligheidsprofiel is Rituximab een eerstelijnsmiddel in de basisbehandeling van NMOSD geworden. De bijwerkingen zijn voornamelijk reacties op infusies en een afname van het aantal witte bloedcellen, die soms gepaard gaat met een afname van het aantal immunoglobulinen (antilichamen die ons beschermen tegen infecties). Regelmatig gebruik van Rituximab is in België pas iets meer dan 2 jaar mogelijk.
Mycofenolaatmofetil (MMF)
MMF werd aanvankelijk gebruikt om afstoting bij transplantatiepatiënten tegen te gaan. Het molecuul heeft een remmend effect op celproliferatie, in het bijzonder op lymfocyten, maar ook op macrofagen en dendritische cellen. MMF vermindert de productie van antilichamen. De gebruikelijke dosis is 1500 tot 3000 mg per dag, verdeeld over twee innames. Het gunstige effect van MMF op NMOSD werd enkel retrospectief geëvalueerd, met vrij variabele, maar over het algemeen positieve resultaten. Het geneesmiddel heeft vaak enkele maanden nodig om zijn volledige werkzaamheid te bereiken. Het wordt ook vaak gecombineerd met corticosteroïden, vooral in het begin van de behandeling. Er werd melding gemaakt van 15 tot 25 % intolerantie, voornamelijk in de vorm van spijsverteringsstoornissen of infecties.
Azathioprine (AZA)
Dit geneesmiddel werd vanaf de jaren 1960 aanvankelijk eveneens gebruikt om afstoting tegen te gaan. Het is een prodrug die door het lichaam wordt omgezet in actieve moleculen. Die moleculen hebben een remmend effect op de proliferatie van lymfocyten, met een verminderde synthese van antilichamen. De doses variëren tussen 1 en 4 mg/kg/dag. Spijsverteringsintolerantie komt relatief vaak voor (4 %). Ernstige infecties en levertoxiciteit worden eveneens gemeld in 2 % van de gevallen. Toediening van corticosteroïden gedurende 3 tot 6 maanden is noodzakelijk om volledige werkzaamheid van AZA te bereiken. De wetenschappelijke gegevens over de relatieve werkzaamheid van AZA zijn nogal tegenstrijdig in vergelijking met MMF of Rituximab.
Mitoxantron (MITOX)
Dit geneesmiddel werd oorspronkelijk gebruikt bij chemotherapie tegen bepaalde vormen van kanker (vooral borstkanker). De immunologische effecten van het middel zijn breed: remming van de werking van B-lymfocyten (waaronder het afscheiden van antilichamen), remming van bepaalde soorten T-lymfocyten en verminderde productie van ontstekingsbevorderende cytokinen (die de communicatie verzorgen tussen de actoren van de immuunreactie). Verschillende wetenschappelijke publicaties melden aanzienlijke gunstige effecten op NMOSD, maar de reeksen zijn meestal vrij beperkt en allerlei verstorende factoren bemoeilijken de interpretatie van de resultaten. Het risico op inductie van leukemie wordt na tien jaar geschat op 1 %, wat het gebruik van dit geneesmiddel momenteel aanzienlijk beperkt.
Cyclofosfamide (CYC)
CYC is eveneens een prodrug die de celdeling verstoort. Het immunosuppressieve effect is breed, zowel op B-lymfocyten als op T-lymfocyten. Het middel heeft ook een modificerende en regulerende werking op de immuunbalans. Cyclofosfamide werd voor het eerst toegepast bij NMOSD om patiënten te behandelen die verschillende auto-immuunziekten vertoonden in verband met de aandoening (lupus, de ziekte van Sjögren). Het aantal gemelde gevallen is beperkt. De gebruikelijke orale dosis is 50 mg per dag.
Geneesmiddelen van de nieuwste generatie en in ontwikkeling
Inebilizumab (MEDI-551)
Inebilizumab is een gehumaniseerd cytotoxisch monoklonaal antilichaam gericht tegen CD19, van type IgG1 kappa. De toxische werking op lymfocyten is afhankelijk van de activering van het complementsysteem en is theoretisch gezien breder dan bij Rituximab. In 2019 werd een fase II-studie gepubliceerd in een toonaangevend wetenschappelijk tijdschrift (The Lancet). Deze studie bracht 230 patiënten samen die werden behandeld met het actieve middel of een placebo. De rekrutering in de dubbelblinde fase werd vroegtijdig stopgezet, omdat al snel werd aangetoond dat het middel een significant gunstig effect en een goed veiligheidsprofiel had.
Satralizumab (SA237)
Satralizumab is eveneens een gehumaniseerd monoklonaal antilichaam (IgG2) dat is gericht tegen interleukine-6. Interleukine-6 is een ontstekingsbevorderend cytokine dat grotendeels wordt gesynthetiseerd door B- en T-lymfocyten, maar ook door monocyten en fibroblasten. Het is een middel dat sterk lijkt op Tocilizumab, een ander monoklonaal IL6-antilichaam dat wordt gebruikt in de reumatologie. De werking heeft niet alleen invloed op de cellen die antilichamen produceren, maar ook op de permeabilisatie van de bloed-hersenbarrière. In november 2019 werd in het New England Journal of Medicine (NEJM) een fase III-studie gepubliceerd die aantoonde dat Satralizumab een uitgesproken gunstig effect had in vergelijking met placebo. De studie werd uitgevoerd bij 83 patiënten, die bovendien een klassieke immunosuppressieve behandeling kregen.
Eculizumab
Nog een gehumaniseerd monoklonaal antilichaam dat zich dit keer bindt aan het terminale deel van een component van het complementsysteem (C5). Het middel veroorzaakt een blokkering van de ontstekingsbevorderende route. Eculizumab werd in de VS al goedgekeurd voor andere auto-immuunziekten (paroxysmale hemoglobuniurie, atypisch hemolytisch uremisch syndroom en myasthenia gravis). In 2019 werden de resultaten van een placebogecontroleerde fase III-studie gepubliceerd in het NEJM. Ze waren uitgesproken gunstig. In februari 2021 werd een tussentijdse analyse van de gegevens van het uitbreidingsonderzoek gepubliceerd in een ander prominent internationaal wetenschappelijk tijdschrift (Annals of Neurology). Een redactioneel commentaar rapporteerde over de zeer positieve effecten en benadrukte dat patiënten moeten worden gevaccineerd tegen meningokokken vóór gebruik van dit geneesmiddel, aangezien ze een hoger risico lopen op deze ernstige infectie. Momenteel wordt geprobeerd om het middel te modificeren en de toedieningsfrequentie te verlagen.
Middelen in ontwikkeling
Ublituximab is nog een monoklonaal CD20-antilichaam dat is gericht tegen cellen die antilichamen produceren. Een complementaire behandeling (combinatie met corticosteroïden) van NMO-opflakkeringen leverde recent nieuwe gegevens op. Momenteel worden nog andere monoklonale CD19-antilichamen of T-cellen die antilichaamproducerende cellen (CAR-T-cellen) kunnen vernietigen, geëvalueerd. Een aantal middelen bevinden zich in een vroeg ontwikkelingsstadium, elk met verschillende werkingsmechanismen. Een voorbeeld is Aquaporumab, een monoklonaal antilichaam dat zich bindt aan dezelfde receptor als het pathologische antilichaam (AQP4Ab), maar een hogere affiniteit heeft. Nog belangrijker is dat het de aanvalsmechanismen van de doelcel blokkeert. Het middel is dan ook bedoeld om te concurreren met het pathologische antilichaam en het zo te blokkeren. Een andere onderzoekspiste richt zich op het herstellen van de integriteit van de bloed-hersenbarrière. Hiertoe wordt onder meer Bevacizumab gebruikt. Dit middel wordt ingezet tegen kanker en blokkeert een stof die de ontwikkeling van nieuwe bloedcapillairen (VEGF) bevordert. Studies bij een klein aantal patiënten wezen op een gunstig effect bij de behandeling van opflakkeringen, in combinatie met corticosteroïden. Ander onderzoek is gericht op de polynucleairen die betrokken zijn bij de ontstekingscascade die aan de basis ligt van NMO-laesies. Een geneesmiddel dat wordt gebruikt bij ernstige acute ademhalingsziekten, zou interessant kunnen zijn vanwege zijn werking op polynucleaire neutrofielen. Cetirizine, een ‘eenvoudig’ antihistaminicum, zou door zijn werking op eosinofielen een gunstig effect kunnen hebben en het risico op recidief beperken. Er gaan een aantal kleinschalige studies in die richting, maar bredere bevestiging is nodig. Bortezomib is een geneesmiddel dat door oncologen wordt gebruikt. Het middel remt het proteasoom, een complex systeem van celoverleving. Het werd getest bij enkele NMO-patiënten die ongevoelig zijn voor Azathioprine of Rituximab, met interessante resultaten.
Tot besluit
De afgelopen vijftien jaar is NMOSD uitgegroeid tot een apart onderzoeksgebied. Er werd inzicht verworven in de belangrijkste pathofysiologische mechanismen, die duidelijk verschillen van die van MS. Door het bestaan van abnormale antilichamen aan te tonen, konden veel nauwkeurigere farmacologische benaderingen worden uitgewerkt. Door klinisch onderzoek internationaal te coördineren, konden studies met een hoge wetenschappelijke waarde worden uitgevoerd. Ze veranderen het paradigma van de behandeling van deze ziekte volledig. De komende jaren zullen patiënten beschikken over nieuwe geneesmiddelen en een geoptimaliseerde behandeling. De sombere functionele prognose waarmee ze in het verleden werden geconfronteerd, zal er volledig anders uitzien.
Dominique Dive, CHU Luik, 21 februari 2021.
Hoofdreferentie en bijbehorend schema: Collongues, N., et al. (2019). "Pharmacotherapy for Neuromyelitis Optica Spectrum Disorders: Current Management and Future Options." Drugs 79(2): 125-142.
Vermoeidheid en multiple sclerose
- Waarin bestaat deze vermoeidheid?
- Hoe valt deze vermoeidheid te verklaren?
- Valt deze vermoeidheid objectief te meten?
- Hoe omgaan met die vermoeidheid?
- Valt vermoeidheid te voorkomen of te behandelen?
- Valt vermoeidheid te verminderen met geneesmiddelen?
Onderzoek verdubbelt het aantal gekende erfelijke risicofactoren voor multiple sclerose
Wetenschappers hebben 29 nieuwe erfelijke risicofactoren voor multiple sclerose (MS) opgespoord en brengen het totale aantal daarmee op meer dan 50. Deze risicogenen hebben weinig voorspellende waarde voor personen met MS of hun familieleden. Het belang ervan ligt evenwel in het genereren van nieuwe inzichten in het ontstaan van de ziekte. Deze grootste genetische studie in MS ooit was eenvoudigweg niet mogelijk zonder een uitgebreid internationaal netwerk van onderzoekers en zonder de deelname van vele duizenden personen die met deze ingrijpende ziekte geconfronteerd worden.
MS is geen erfelijke ziekte, maar er is wel een erfelijke aanleg. Zo komt de ziekte iets meer voor in dezelfde families: één op vijf van de personen met MS heeft nog één of meerdere familieleden met de ziekte. De eerste erfelijke risicofactor voor MS werd al ontdekt in de jaren '70. Daarna bleek het - ondanks veel inspanningen - moeilijk om vooruitgang te boeken. Sinds enkele jaren beschikken we echter over de kennis en de instrumenten die de sleutels bleken te zijn tot succesvolle genetische studies.
Een internationaal team van onderzoekers bundelden nu hun krachten in een samenwerkingsverband met de naam Internationaal Multiple Sclerose Genetica Consortium en Wellcome Trust Case Control Consortium. Het team werd geleid door de universiteiten van Cambridge en Oxford. In België werkten wij vanuit het Laboratorium voor Neuroimmunologie van de K.U.Leuven met mee aan dit onderzoek. We rapporteerden onze bevindingen op 11 augustus in het gerenommeerde wetenschappelijke tijdschrift Nature. Het is meteen de grootste genetische studie over MS ooit. Bijna 250 onderzoekers uit verschillende landen bestudeerden het erfelijk materiaal of DNA van 9772 personen met MS en 17376 gezonde controlepersonen uit 15 verschillende landen. Daarbij waren ook meer dan 500 personen met MS die in de Universitaire Ziekenhuizen Leuven of het Nationaal Multiple Sclerose Centrum in Melsbroek door het geven van een bloedstaal meewerkten aan dit onderzoek.
Eerst bevestigden we de rol van 23 eerder gekende erfelijke risicofactoren. Daarnaast identificeerden we 29 nieuwe erfelijke variaties die mee de aanleg voor de ziekte bepalen, wat het totaal aantal gekende erfelijke risicofactoren verdubbelt tot meer dan 50.
Een groot aantal van deze risicofactoren zijn variaties in genen die een sleutelrol spelen in het afweersysteem, bijvoorbeeld in de functie van de T-cellen (een type van witte bloedcellen dat verantwoordelijk is voor de afweer tegen bacteriën of virussen maar ook een rol speelt in de reactie tegen het eigen lichaam in auto-immuunziekten) en de activatie van interleukines (boodschapper-eiwitten tussen verschillende types afweercellen). Opmerkelijk is dat voor een derde van de risicofactoren voor MS een rol in de aanleg voor andere auto-immuunziekten (zoals de ziekte van Crohn en type 1 diabetes) al gekend was. Dit toont aan dat dezelfde mechanismen een rol spelen in meer dan één type auto-immuunziekte.
Eerder onderzoek suggereerde een verband tussen vitamine D tekort en een verhoogd risico op MS (zie Nieuwsbrief nr. 29 mei 2011). In deze studie vonden we nu, naast de risicofactoren die een directe rol spelen in het immuunsysteem, ook twee risicofactoren die zorgen voor de omzetting van vitamine D. Dit leidt tot meer inzicht in het verband tussen erfelijke factoren en omgevingsfactoren die beide een rol spelen in MS.
De mate waarin de erfelijke risicofactoren het risico van een persoon op MS verhogen, is te klein om bruikbaar te zijn voor voorspellingen over wie de ziekte wel of niet zal krijgen. Het gaat hier niet om zeldzame ‘foutjes' in het erfelijk materiaal zoals we dat bij erfelijke ziekten zoals bepaalde kankers zien. Het gaat wel om normale variatie tussen mensen. Die normale variatie bepaalt mee allerlei eigenschappen van personen, zoals de kleur van haar en ogen, de aanleg voor zwaarlijvigheid of de aanleg voor ziekten zoals MS. Iemand die veel erfelijke risicofactoren voor MS draagt, heeft iets meer kans om de ziekte te krijgen dan iemand die minder erfelijke risicofactoren draagt.
Het ontrafelen van de basis voor de erfelijke aanleg voor een ziekte zorgt voor betrouwbare inzichten in de ziektemechanismen. Zo laat deze studie toe te zien welke cellen en eiwitten van het afweersysteem cruciaal zijn in het ontstaan van de ziekte. Deze kennis is van belang voor een beter begrip van MS en het verbeteren van de behandeling. Dit wordt geïllustreerd doordat twee van de erfelijke risicofactoren het doelwit zijn van al bestaande behandelingen. De andere risicofactoren kunnen nieuwe doelwitten voor toekomstige behandelingen aanwijzen.
De grote vooruitgang die gemaakt is met deze studie opent nieuwe wegen in het onderzoek over MS. We moeten nu bestuderen hoe deze erfelijke risicofactoren - alleen of in combinaties - hun effect op de aanleg voor de ziekte precies uitoefenen en hoe we hierop kunnen inwerken om MS op de best mogelijke manier te behandelen.
Prof A. Goris1
Prof B. Dubois1, 2
1Laboratorium voor Neuroimmunologie, Departement Neurowetenschappen, KULeuven
2Dienst Neurologie, Universitaire Ziekenhuizen Leuven
Nieuwe therapeutische mogelijkheden in MS
Multiple sclerose is een aandoening waarbij twee processen voorkomen. Het eerste is een intermittente ontsteking, nl. klinische opstoten of "actieve" letsels (inflammatoire lesie die intraveneus geinjecteerd contrast capteert) op beeldvorming (MRI), niet steeds klinisch opgemerkt. Het tweede proces is een langzame degeneratie van zenuwvezels beroofd van hun myelineschede, of vernietigd langs hun verloop door de initiële ontsteking.
De nieuwe behandelingen die opdoemen aan de horizon zijn in wezen anti-inflammatoire, en bieden geen bescherming jegens de neuro-degeneratie, secundair op reeds ontwikkelde inflammatoire letsels. Ze leiden evenmin tot een herstel van de myelineschede. Ze zullen de ziekte beter dan vandaag stabiliseren. Als er verbetering van een bestaande toestand optreedt, is het dan ook te danken aan het 'spontaan, natuurlijk' herstel waarbij remyelinisatie in letsels zich voordoet na het verdwijnen van de ontsteking. Helaas blijkt dit natuurlijke herstel veelal ontoereikend en wordt het overweldigd door de omvang van de laesies. Therapeutische trials bij progressieve vorm van MS (hetzij onmiddellijk zonder opstoten di. primair of secundair na fase met opstoten) zijn niet succesvol gebleken.
Momenteel beschikken we bij de opstootsvorm van MS over beta-interferon (Avonex, Betaferon, Rebif en Extavia) en glatirameer acteaat (Copaxone), met beide een verschillend werkings-mechanisme. Deze 5 producten vormen de basisbehandeling en worden alle via injectie (onderhuids of in spier) toegediend. Zij vertonen globaal dezelfde efficaciteit bij groepsvergelijking. Doch individueel bestaan grote verschillen, er zijn "goede", "gemiddelde" en "niet"-responders bij elke behandeling. Bij "goede" respons zal de frequentie van exacerbaties halveren, de ernst van de resterende opstoten is eveneens beduidend geringer en de laesies MRI nemen slechts met een paar procent toe over 5 jaar (itt. 27% in de afwezigheid van behandeling). Op middellange (5 jaar) en lange termijn (20 jaar), blijken deze medicaties uiterst veilig en zonder ernstige bijwerkingen te zijn.
Bij een onvoldoende respons (ernstige opstoten, ernstige deterioratie op MRI, talrijke actieve letsels op MRI) bij adequate behandeling met deze eerste lijn medicaties, gebruiken we natalizumab (Tysabri), intraveneus toegediend om de 4 weken. Deze medicatie blokkeert de doorgang van lymfocyten (belangrijkste cellulaire afweercellen) vanuit de bloedbaan naar de hersenen of het ruggenmerg. Het is momenteel de meest effectieve behandeling bij zeer actieve opstootsvorm van MS. Helaas is er een risico, weliswaar laag maar reëel, op de ontwikkeling van encefalitis (herseninfectie) veroorzaakt door een virus dat de hersenen binnendringt en de myeline producerende cellen vernietigt. Er is geen medicijn tegen het virus. Wij geven Tysabri dan ook enkel als we overtuigd zijn dat de voordelen het risico van encefalitis in belangrijke mate overtreffen. Ten slotte kan Novantrone (intraveneuse toediening) overwogen worden bij personen met opstoten en progressieve verslechtering van de aandoening, geassocieerd met persisterend nieuwe en actieve letsels bij beeldvorming. Bij de keuze voor Novantrone dient echter terdege rekening gehouden worden met een hoge toxiciteit (hartfalen, leukemie, ...).
De nieuwe medicijnen situeren zich op hetzelfde niveau als eerste lijn medicaties, of tussen deze en Tysabri : ze zullen net zo effectief zijn of effectiever dan de huidige eerste lijn, en makkelijker gezien orale inname (pil). Bijwerkingen op korte en middellange termijn zijn echter onbekend. Er zal geen reden zijn om de behandeling van een persoon die de injecties van de huidige producten goed verdraagt, en in remissie is zowel klinisch als radiologisch (beeldvorming van de hersenen en het ruggenmerg) te veranderen.
1. Gilenya ® (Fingolimod), 1 capsule per dag, beinvloedt de stroom van lymfocyten in de bloedbaan en richt ze naar de lymfeklieren. Op deze manier wordt voorkomen dat lymfocyten de barrière tussen bloed en hersenen kruisen. De gepubliceerde resultaten zijn sterk positief. Het werd aanvaard door de Amerikaanse Food & Drug Administration als eerste lijn behandeling en door het Europese agentschap EMEA bij mislukking van de eerste lijn, analoog aan de registratiecriteria bij Tysabri. Het moet nu worden voorgelegd aan de gezondheidsautoriteiten van elk Europees land, wat in België toch even kan duren. Het zou in elk geval onaanvaardbaar zijn dat de indicaties weerhouden in België strenger zijn dan de Europese voorwaarden, zoals oorspronkelijk ook het geval was bij Tysabri.
2. Cladribine is een immunosuppressivum oraal toegediend die slechts enkele dagen per jaar dient ingenomen gezien zijn lange werkingsduur. Het Europees Agentschap heeft dit product niet weerhouden ter behandeling van MS, uit angst voor de lange termijn risico's. De gepubliceerde resultaten zijn weliswaar zeer positief, doch verdere lange termijn studies dienen afgewacht.
3. Fumaraat (BG12), teriflunomide en laquinimod zijn eveneens medicaties die oraal worden toegediend. De efficaciteit is ten minste vergelijkbaar met de huidige eerste lijn medicatie, zoals blijkt uit de recent afgeronde investigaties.
Ten slotte zijn nog talrijke medicijnen in onderzoek met een nog ingrijpender invloed op het ziekteproces vanaf de eerste manifestatie en gericht op "heropstart" van het immuunsysteem. Dit is alentuzumab (Campath) en antistoffen gericht tegen B-cellen nl. rituximab en ocrelizumab.
De conclusie is duidelijk. Binnen 5 jaar zal de behandeling bij MS ingrijpend veranderen. Bij elke patiënt(e) zal echter de balans tussen risico's, voordelen, kwaliteit van leven, persoonlijke projecten (bijvoorbeeld zwangerschap) dienen afgewogen te worden. In de komende 5 jaar is er bovendien nog veel onderzoek noodzakelijk om de progressieve vormen van de ziekte af te remmen en zo mogelijk de reeds aanwezige schade te herstellen.
Professor C. Sindic
(vertaling Dr. D. Decoo)
Mei 2011
Een nieuw tijdperk voor de behandeling van MS?
Op 12, 13 en 14 november 2009 vond in Lissabon de vergadering plaats van de Europese Charcot stichting. Deze organisatie verenigt talrijke experten in MS met als doel stil te staan bij de nieuwe wetenschappelijke inzichten en de nieuwe behandelingen die hier eventueel uit kunnen voortkomen.
Het is onmogelijk om zelfs gedeeltelijk alles weer te geven wat er werd gezegd tijdens deze vergadering, maar de aandacht werd vooral door 2 belangrijke elementen getrokken:
- - Eerste element
Het basiswetenschappelijk onderzoek rond MS heeft vooral geleid tot een enorme hoeveelheid aan nieuwe informatie over de mechanismen van de ziekte op moleculair biologisch niveau. Deze informatie is nodig om andere aanknopingspunten te vinden voor de ontwikkeling van nieuwe behandelingen, maar leidt natuurlijk niet onmiddellijk tot nieuwe therapieën.
- - Tweede element
Nieuwe behandelingen worden onderzocht bij personen met MS. Verschillende van deze studies zijn reeds in fase III (voor registratie), en definitieve resultaten worden de komende 3 jaren verwacht. Zelfs indien niet al deze studieproducten het zullen brengen tot een behandeling voor MS, kan men toch hopen dat er op relatief korte termijn nieuwe producten op de markt zullen komen, waarvan sommige langs de mond kunnen worden ingenomen.
Nieuwe producten
De producten waarvan het meest gesproken wordt, zijn vanzelfsprekend die waarvan de studies het verst staan. Verschillende van deze producten worden immers al maanden toegediend aan personen met MS die in een studie zeer nauwkeurig worden opgevolgd, zowel wat de klinische evolutie van hun ziekte betreft (aantal aanvallen, evolutie van de handicap), als wat de evolutie bij bepaalde technische onderzoeken betreft (herhaalde beeldvorming).
De producten die momenteel het verst in de ontwikkeling staan zijn:
- - CLADRIBINE
- - FINGOLIMOD
- - LAQUINIMOD
- - FUMARAAT
- - ALEMTUZUMAB
- - PIXANTRONE
- - een STATINE...
(niet-exhaustieve lijst)
In deze tekst zullen wij jullie meer informatie geven over cladribine, fingolimod en laquinimod, waarvan de studie reeds goed gevorderd is. Op de andere producten zal worden teruggekomen wanneer meer gedetailleerde resultaten beschikbaar zijn.
CLADRIBINE
Cladribine wordt reeds jaren gebruikt in de behandeling van leukemie. Na een kortdurende toediening via orale weg, vermindert cladribine in belangrijke mate en tevens langdurig het aantal circulerende T-lymfocyten. Bij patiënten met relapsing-remitting MS gaat deze daling van witte bloedcellen gepaard met een duidelijke vermindering van de aanvalsfrequentie en van het aantal nieuwe letsels dat met een hersenscan (MR) kan worden in het licht gesteld. Dit gunstige effect is minstens even sterk zoniet sterker dan dat van interferon-beta, alhoewel dit laatste nog moet worden aangetoond in een vergelijkende studie.
Het voordeel van cladribine is dat het werkingsmechanisme verschilt van dat van interferon-beta en glatirameer acetaat. Hierdoor zou het mogelijk zijn dat het werkzaam is bij patiënten die van de andere behandelingen geen gunstig effect ondervinden.
FINGOLIMOD
Fingolimod is een sfingosine-analoog. De binding van fingolimod aan de sfingosinereceptor aan de oppervlakte van de T-lymfocyten zorgt ervoor dat de aggressieve T-cellen vastgehouden worden in de lymfeklieren. Bij personen met relapsing-remitting MS leidt dit tot een belangrijke daling van de aanvalsfrequentie en van het aantal nieuwe letsels dat bij beeldvorming van de hersenen wordt vastgesteld. In een studie bij meer dan 1000 patiënten die gedurende 1 jaar werden behandeld, bleek fingolimod een beter effect te hebben dan een interferon-beta.
Zoals voor cladribine is een pluspunt van dit product zijn werkingsmechanisme. Hierdoor is het mogelijk dat patiënten die niet goed reageren op de standaardtherapieën wel een gunstig effect hebben op fingolimod. Bovendien is fingolimod een pil, wat uiteraard ook een voordeel is.
LAQUINIMOD
Laquinimod is een kleine molecule die de verhouding tussen Th1 en Th2 lymfocyten wijzigt. Hierdoor neemt het relatieve aantal Th2 cellen toe en dus ook de hoeveelheid cytokinen die door deze laatste cellen worden geproduceerd.
Men weet dat de ontsteking die de hersenletsels veroorzaakt bij personen met MS afhankelijk is van bepaalde cytokinen. Sommige cytokinen stimuleren de ontsteking (pro-inflammatoire cytokinen, geproduceerd door Th1 cellen), andere remmen de ontsteking af (anti-inflammatoire cytokinen, geproduceerd door Th2 cellen).
Ook laquinimod heeft een werkingsmechanisme dat volledig verschilt van dat van de bestaande en beschikbare behandelingen.
Ongewenste effecten van de nieuwe producten
Zoals iedereen weet, is een belangrijk punt bij de goedkeuring van nieuwe producten door de registratiecommissies het feit dat ze goed verdragen moeten worden. Niet alleen moet het nieuwe product werkzaam zijn, het mag ook niet gevaarlijk of toxisch zijn.
Hoe zit het met de nieuwe producten die hierboven beschreven zijn ? Hierbij moet het volgende voor ogen worden gehouden: indien het aantonen van de therapeutische werking moeilijk en kostelijk is voor de laboratoria, dan is het aantonen van het feit dat het product goed verdragen wordt een nog veel meer veeleisende zaak. Verschillende honderden patiënten moeten minstens 2 jaar behandeld zijn om iets te kunnen zeggen over de efficiëntie van het product, maar duizenden patiënten, gedurende veel langere periodes behandeld, zijn nodig om de schadeloosheid van een nieuw product aan te tonen.
Dit betekent dat heel wat nieuwe geneesmiddelen op de markt komen voor men volledige zekerheid heeft over het ontbreken van ongewenste effecten op lange termijn. Dit betekent dat patiënten die dergelijke producten krijgen heel nauwkeurig moeten gevolgd worden, vooral als het een product betreft dat werkt op het immuunsysteem. Met dit soort van geneesmiddelen immers kunnen er infectieuze verwikkelingen optreden, zoals progressieve multifocale leukoencefalopathie (ernstige virale herseninfectie). Een nauwkeurige opvolging is dus nodig om deze mogelijke ongewenste effecten op te sporen en de gevolgen ervan zo goed mogelijk te beperken.
Besluit
De behandeling van MS zal binnenkort verrijkt worden met nieuwe producten die beschikken over andere werkingsmechanismen. Men zal aldus over een therapeutisch arsenaal beschikken, en mogelijk zullen verschillende producten in combinatie worden gebuikt. Dit zal de opvolging van personen met MS zonder twijfel beïnvloeden. Dit is een hoopgevend perspectief, en in Lissabon heerste dan ook een zeker optimisme.
Nochtans vergeten we hiermee niet de dagelijkse moeilijkheden waar vele personen met MS mee worstelen. De artsen vergeten niet dat het leven met MS een ware uitdaging kan betekenen voor de personen met MS en hun omgeving. Voor hen gaat de vooruitgang begrijpelijkerwijze nooit snel genoeg.
Dr.J.P. Rihoux
(vertaling Prof. B. Dubois)
Februari 2010
Multiple sclerose en vaccinaties
De Medische Adviesraad van de Nationale MS-Liga evalueerde tijdens de vergadering van 6 oktober 2009 de vragen omtrent vaccinatie bij personen met multiple sclerose. Dit gebeurde in het licht van het griepepidemie risico met het nieuwe virus A/H1N1.
De Medische Adviesraad wenst volgende punten te benadrukken :
- Bij geen enkele vaccinatie heeft men negatieve effecten vastgesteld na toediening bij personen met multiple sclerose. Geen enkele vaccinatie ligt aan de basis van een ontwikkeling, een opstoot of een verergering van multiple sclerose. Het tetanus vaccin heeft mogelijks een beperkt beschermend effect.
- Het vaccin jegens seizoensgriep is specifiek geëvalueerd. Hij wordt goed getolereerd & veroorzaakt geen MS opstoten of nieuwe activiteiten op magnetische resonantie beelden. Bij een griepepidemie vertonen gevaccineerde patiënten beduidend minder opstoten dan niet gevaccineerde patiënten.
- Personen met MS zijn niet kwetsbaarder of meer bedreigd door het nieuwe A/H1N1 virus dan de algemene populatie.
- Er is geen enkel element dat laat vermoeden dat het vaccin jegens het nieuwe griepvirus minder goed getolereerd wordt of gevaarlijker is dan het klassieke vaccin jegens seizoensgriep.
- Personen met MS, waarbij door huisarts of neuroloog de klassieke griepvaccinatie wordt geadviseerd, kunnen dan ook gebruik maken van het vaccin jegens het nieuwe virus A/H1N1. Een interval tussen beide vaccinaties van 3 tot 4 weken dient gerespecteerd.
- Het vaccin jegens seizoensgriep en A/H1N1 kan zonder problemen toegepast worden bij patienten onder behandeling met beta-interferones (Avonex, Betaferon, Rebif), Copaxone en Tysabri, evenals Novantrone, Imuran en Ledertrexate. Bij deze laatste 3 medicaties kan het vaccin echter wel iets minder efficiënt zijn. Hoe dan ook verzekert het vaccin nooit een 100% protectie.
Oktober 2009
Alemtuzumab
Persartikels mbt alemtuzumab :
Op 23 oktober jl. werden de resultaten bekend gemaakt van een fase 2 studie met alemtuzumab in relapsing-remitting multiple sclerose. Het middel werd ontwikkeld aan de universiteit van Cambridge, en recent onderzocht in een studie met 334 patiënten.
Twee derden van de deelnemende patiënten werden behandeld met het studieproduct alemtuzumab (1/3 lage dosis, 1/3 hoge dosis) en één derde kreeg een standaardtherapie met Rebif. De aanvalsfrequentie werd met 74% verminderd in de alemtuzumab behandelde patiënten. 80% van de met alemtuzumab behandelde patiënten bleef aanvalsvrij gedurende 3 jaar, terwijl dit in de Rebif groep 52% was.
Bij de alemtuzumab behandelde patiënten werd zelfs een verbetering vastgesteld in de functionele mogelijkheden, terwijl de met Rebif behandelde groep een verdere ziekte-evolutie onderging. De belangrijkste bijwerkingen waren infecties, auto-immuun schildklierlijden, en zeldzaam een auto-immuun tekort aan bloedplaatjes waardoor éénmaal een fatale hersenbloeding optrad.
Deze gunstige resultaten zijn de aanleiding om het gebruik van alemtuzumab verder te onderzoeken in een grotere fase 3 studie, die momenteel ook in ons land loopt. Indien deze hoopvolle resultaten bevestigd worden, zal alemtuzumab in de toekomst wellicht de behandelingsmogelijkheden voor personen met MS verruimen.
Alternatieve therapieën in MS: een waardig alternatief?
Het gebruik van alternatieve therapieën in multiple sclerose (MS) is populair maar controversieel. Aangezien alternatieve geneesmiddelen/geneeswijzen niet zeldzaam worden toegepast in MS - alleen of in combinatie met een conventionele therapie - is het zinvol even te blijven stilstaan bij hun betekenis en plaats in de behandeling van MS.
Alternatieve therapieën zijn behandelingen waar weldoende effecten aan worden toegekend bij allerlei ziekten en ziektetekens, zonder dat hiervoor echt het bewijs werd geleverd dat ze ook echt werkzaam zijn en dat de eventuele bijwerkingen aanvaardbaar zijn. In MS kan men de alternatieve therapieën schematisch in twee groepen indelen: deze met een vermeend effect op het ziekteverloop en deze waarvan men denkt dat ze bepaalde symptomen of klachten kunnen verlichten.
Alternatieve geneeswijzen zijn vooral in trek in aandoeningen waarvoor geen afdoende behandeling bestaat. Het spreekt voor zich dat men sneller zijn toevlucht zoekt in onbewezen behandelingen indien men lijdt aan een langdurige, ongeneeslijke ziekte, zoals bijvoorbeeld MS. Heel wat personen met MS (50-60%) zouden dan ook ooit in hun ziekteverloop gebruik maken van alternatieve geneeswijzen, soms tijdelijk, soms gedurende een langere periode. In een Duitse studie met 254 personen met MS bleken gebruikers van alternatieve geneeswijzen gemiddeld 44 jaar te zijn met een gemiddelde ziekteduur van iets meer dan 8 jaar. Hun gemiddelde EDSS score bedroeg 4, wat betekent dat ze nog in staat zijn 500m te stappen zonder hulpmiddelen. Geslacht, opvoeding, geloofsovertuiging speelden hierbij geen rol. Wel hadden gebruikers van alternatieve therapieën een langere ziekteduur, een hogere EDSS en waren ze ouder dan de personen die geen gebruik maakten van alternatieve geneeskunde.
Het is onmogelijk om een volledige lijst te geven van alle mogelijke alternatieve geneeswijzen in MS. Enerzijds zijn er therapieën die het ziekteverloop zouden beïnvloeden, zoals bepaalde diëten, rijk aan polyonverzadigde vetzuren of anti-oxidantia. Anderzijds zijn er behandelingen die vooral trachten symptomen te verlichten. Hierbij denken we aan afkoeling, acupunctuur, yoga, en tenslotte zijn er therapieën die via beide mechanismen zouden inwerken: cannabis, gingko biloba, vitamine D. Sommige van deze behandelingen lijken veelbelovend, andere zijn schadelijk, maar van alle is het effect onvoldoende aangetoond.
Sommige alternatieve geneesmiddelen kunnen zeker nuttig zijn, maar jammer genoeg werd dit voordelig effect nooit bewezen. Voor de meeste van deze therapieën werd er nooit een studie gestart, voor andere kon de uitgevoerde studie op onvoldoende overtuigende wijze aantonen dat de behandeling een gunstig effect had.
Aangezien niet alleen het effect, maar ook de mogelijke bijwerkingen van alternatieve therapieën onvoldoende werden bestudeerd, is het zeker niet uitgesloten dat sommige alternatieve therapieën schadelijk zouden zijn. Naast een mogelijk rechtstreeks schadelijk effect, sluipt ook het gevaar van een ongecontroleerd gebruik van deze therapieën, waardoor op zich onschadelijke behandelingen, misschien toch schadelijk zouden kunnen zijn. Tenslotte is de kostprijs van deze behandelingen vaak niet in verhouding tot het gunstig effect dat men ervan zou kunnen ondervinden.
Het gebruik van alternatieve middelen in de behandeling van MS is wijd verspreid. Het is niet uitgesloten dat sommige van deze toepassingen inderdaad het ziekteverloop kunnen moduleren of bepaalde klachten kunnen verlichten. Het zou echter verstandiger zijn deze middelen eerst te onderwerpen aan dezelfde strikte voorwaarden waaraan 'klassieke geneesmiddelen' moeten voldoen vooraleer er - vaak op ongecontroleerde wijze - gebruik van te maken.
|
Stress en MS
|
Al meer dan 100 jaar geleden haalde Charcot aan dat psychologische stress een MS opflakkering kan uitlokken. De meeste personen met MS ondervinden dat stressvolle gebeurtenissen een rol kunnen spelen in het optreden van MS aanvallen. De voorbije jaren werden hierover heel wat studies gepubliceerd. Ook de NMR scan van de hersenen werd ingeschakeld.
In een recente studie over stress, trauma en MS werden de gegevens van 20 eerder gepubliceerde studies (periode 1965-2003) kritisch onderzocht. Na grondig onderzoek van de kwaliteit van deze studies, voldeden 14 van hen aan de criteria om gegevens samen te brengen (meta-analysis). In 13 van de 14 studies werd een gelijkaardig effect aangetroffen van stress op MS aanvallen: de kans op aanvallen neemt toe in aansluiting op een stressvolle levensgebeurtenis. De grootte van het effect is matig maar klinisch betekenisvol. In één studie bleek het tegenovergestelde: tijdens de eerste Golfoorlog lokten de raketaanvallen in Tel Aviv minder MS opflakkeringen uit! Verschillende soorten stressoren kunnen dus een verschillend effect hebben op de MS aanvallen.
In een tweede studie werd de gezondheid van Deense ouders onderzocht die een kind verloren hadden dat jonger was dan 18 jaar. Hun gezondheid werd vergeleken met deze van een groep ouders die geen kind verloren hadden. Het risico om MS te ontwikkelen bleek voor de ouders die een kind verloren hadden de helft hoger dan voor de ouders die geen kind verloren hadden. Dit verband werd pas duidelijk na verloop van 8 jaar. Indien het verlies van een kind onverwacht kwam, bleek het risico om MS te ontwikkelen verdubbeld. Deze resultaten suggereren dat een extreem stressvolle gebeurtenis zoals het verlies van een kind het risico op MS beïnvloedt.
Deze studieresultaten openen mogelijkheden voor het onderzoek naar de psychologische, neurohormonale en immunologische gevolgen van stressvolle levensgebeurtenissen op MS. Hieruit mag niet besloten worden dat personen met MS hun lot zelf zouden kunnen bepalen.
|
|
De immunomodulerende eigenschappen van statines, cholesterolverlagende medicijnen, zijn reeds langer bekend.
Recent bleken deze medicijnen het begin van experimentele allergische encefalomyelitis (EAE), het diermodel voor MS, uit te stellen en de ernst van deze ziekte te verminderen. Bij proeven op menselijke witte bloedcellen werden de onstekingsverschijnselen sterk afgeremd. Een eerste, kleine studie bij relapsing remitting MS heeft bemoedigende resultaten. Onder een hoge dosis simvastatine (80 mg) wordt een vermindering van het aantal actieve letsels op de NMR hersenen gezien. Grotere klinische studies zijn nodig om de veiligheid en effectiviteit van deze producten bij MS te bepalen.
|
MS en zonlicht
| Multiple Sclerose ontstaat door een samenspel van invloeden afkomstig uit het milieu en van erfelijke kenmerken van de persoon. Verschillende genen (dragers van onze erfelijke eigenschappen) blijken een rol te spelen in het bepalen van het risico op MS, maar slechts enkele ervan zijn gekend. Personen die drager zijn van een of meerdere van deze genen en daardoor een aanleg hebben voor MS zullen echter slechts MS ontwikkelen indien ze worden blootgesteld aan bepaalde invloeden uit de omgeving die MS kunnen uitlokken. Dit zouden sommige virusinfecties kunnen zijn of schadelijke stoffen of tekorten in de voeding of nog andere factoren. We weten er echt weinig over. Daarom is de ontdekking van Ingrid van der Mei dat een gebrek aan blootstelling aan zonlicht een rol kan spelen bij het ontstaan van MS zo belangrijk, al moeten we er aan toevoegen dat vroegere onderzoekers hiervoor ook al aanwijzingen hadden.
Ingrid van der Mei en haar medewerkers ondervroegen in Tasmanië, een eiland onder het Australische vasteland, 136 personen met MS en 272 gezonde personen van vergelijkbare leeftijd en geslacht over een reeks gebeurtenissen en ervaringen in de loop van hun leven. Ze informeerden echter vooral naar de graad van blootstelling aan zonlicht in de loop van de jaren. Een lage graad van blootstelling werd vastgelegd als dagelijks gemiddeld minder dan 2-3 uur, een hoge graad als dagelijks gemiddeld meer dan 2-3 uur expositie. De gegevens van de MS-patiënten werden vervolgens vergeleken met de ervaringen van de ondervraagden die geen MS hadden. Uit de vergelijking kwam naar voor dat een hoge zonexpositie, in de leeftijdsperiode van 6 tot 15 jaar, het risico om later ooit MS te krijgen met meer dan de helft deed dalen. De zonexpositie in de wintermaanden leek het grootste effect te hebben. Verder was het merkwaardig dat op hogere leeftijd, en meer bepaald in de 10 jaren die het optreden van MS vooraf gingen, de graad van expositie aan de zon geen invloed meer had op het risico om MS te ontwikkelen. De resultaten van de enquête worden in zekere zin ondersteund door de bevindingen van een ander deel van de studie: de MS-patiënten vertoonden minder huidbeschadiging door de zon dan de vergelijkingspersonen zonder MS. Deze studie werd zeer zorgvuldig uitgevoerd en lijkt zeer overtuigend, maar het laatste woord daarover is natuurlijk nog niet gezegd. Kritische personen zullen niet nalaten op te merken dat er vraagtekens kunnen worden geplaatst bij de betrouwbaarheid van het geheugen voor de graad van blootstelling aan de zon, zovele jaren geleden in de kinderjaren en jonge adolescentie. Probeer het uzelf maar eens te herinneren. Hierop kan geantwoord worden dat deze studie niet alléén staat en dat resultaten van enkele vroegere studies ook reeds in de richting van invloed van het zonlicht wezen. Een gevolg van deze studies is dat er intens zal gezocht worden naar veranderingen in het lichaam, vooral in de immuniteit, die mogelijk tussenkomen in het effect van het zonlicht op het ontstaan van MS. Dit is niet alléén theoretisch belangrijk, maar ook van belang voor eventuele therapeutische toepassingen. Misschien kan eenzelfde of zelfs groter beschermend effect bereikt worden door in te grijpen op deze tussenliggende mechanismen, eerder dan door meer in de zon te lopen. Kinderen blootstellen aan meer zonlicht heeft niet alléén een mogelijk beschermend effect voor MS, maar heeft zeker ook een schadelijk effect door het verhoogd risico op huidkanker. Aanraden om zeer veel in de zon te lopen zal niemand voorlopig doen, omdat niemand weet of de voordelen zouden opwegen tegen de nadelen. Tenslotte is het belangrijk op te merken dat de studie van Van der Mei alléén het belang van zonlicht in het voorkomen van MS onderzocht. Of zonlicht een invloed heeft op het verloop van de ziekte bij wie reeds MS heeft, werd nog nooit onderzocht. Het verloop van de ziekte beïnvloeden kan dus slechts met medicamenten als interferonen en glatirameer-acetaat die vooral bij het begin van de ziekte een duidelijk, zij het beperkt, effect hebben.
|
Cannabis en multiple sclerose
Cannabis wordt reeds meerdere jaren medicinaal gebruikt in de behandeling van spasticiteit en pijn, oa. bij multiple sclerose (MS). Deze toepassing komt nu steeds meer op de voorgrond gezien de registratie van Sativex® in meerdere Europese landen. Op heden is Sativex® echter nog niet beschikbaar in België.
Sativex® is een tinctuur van de cannabisplant die oraal verstuifd wordt. Elke verstuiving levert een gestandardiseerde dosis van 2.7mg tetrahydrocannabinol (THC) en 2.5mg cannabidiol (CBD). De registratie van Sativex® volgt op enkele studies die argumenten boden voor een reductie van spasticiteit in personen met MS. Vooral de subjectieve evaluatie van de behandeling detecteerde duidelijke verbetering van de spasticiteit, terwijl de objectieve meting van de spasticiteit vaak geen significant verschil vertoonde (1, 2). De studie die leidde tot de registratie van Sativex® detecteerde wel een significant effect op spasticiteit, maar alleen in de groep van 42% vooraf geselecteerde responders (3). Ook met een andere vorm van medicinale cannabis, nl. een capsule tetrahydrocannabinol, werd recent een effect aangetoond op subjectieve aspecten van spasticiteit zoals de ernst ervan, pijn, en slaapkwaliteit (4).
Er dient duidelijk gewaarschuwd voor het gebruik van niet-medicinale cannabis, zowel gerookt als oraal ingenomen. De hoeveeldheid THC is immers sterk toegenomen. Gemiddeld bedroeg de concentratie in de jaren '60 ongeveer 10mg THC per sigaret, wat nu is opgelopen tot 150mg of meer. Bij roken is er bovendien een snelle opname van minstens 50% en zijn kankerverwekkende effecten beschreven. Cannabis behoudt bovendien een langdurig effect wegens de actieve afbraakproductien en de heropname via darm. Volledige eliminatie van 1 dosis kan tot 30 dagen in beslag nemen (5). De acute toxiciteit van cannabis is weliswaar laag, doch duizeligheid, lichthoofdigheid, psychische & cognitieve stoornissen treden vaker op. Dit laatste is vooral belangrijk bij personen met MS, gezien er in MS reeds cognitieve stoornissen kunnen voorkomen bij 43-65%. Deze cognitieve stoornissen kunnen toenemen bij gebruik van cannabis. Het gebruik van cannabis leidt tot tragere informatieverwerking, lagere alertheid, verminderd werkgeheugen en tragere psychomotore snelheid, vooral wanneer het langdurig gebruikt wordt ( 6-9). Op basis van deze data moet dan ook gewaarschuwd worden tegen het gebruik van niet-medicinale cannabis en is voorzichtigheid zeker ook aangewezen bij eventueel gebruk van medicinale vormen indien reeds cognitieve stoornissen aawezig zijn.
Dr. D. Decoo - oktober 2012
Referenties :
1. Lakhan S et al - Whole plant cannabis extracts in the treatment of spasticity in multiple sclerosis: a systematic review. BMC Neurol 2009, 9:59.
2. Leussink VI et al. Symptomatic therapy in multiple sclerosis: the role of cannabinoids in treating spasticity. Ther Adv Neurol Disorders 2012; 5: 255-266.
3. Novotna A et al. A randomized, double-blind, placebo-controlled, parallel-group, enriched design study of nabiximols (Sativex ®) as add-on therapy in subjects with refractory spasticity caused by multiple sclerosis. - Eur J Neurol, 2011, 18(9): 1222-1131.
4. Zajicek JP et al. Multiple Sclerosis and extract of cannabis: results of the MUSEC trial. JNNP 2012; 83: 1125-1132.
5. Ashton C. Pharmacology and effects of cannabis: a brief review. B J Psychiatry 2001, 178:101-106.
6. Wadsworth E et.al. Cannabis use, cognitive performance and mood in a sample of workers. - J.Psychopharmacol. 2006, 20:14-23.
7. Crean R et al. An evidence-based review of acute and long-term effects of cannabis use on executive cognitive functions. - J.Addict.Med. 2011,5:1-8.
8. Rao S et al. Cognitive dysfunction in multiple sclerosis. I. Frequency, patterns, and prediction. Neurology 1991, 41:685-691.
9. Honarmand K et.al. Effects of cannabis on cognitive function in patients with multiple sclerosis. Neurology 2011, 76:1153-1160.
Verband tussen Hepatitis B-vaccinatie en MS
De Medische Adviesraad van de Nationale Belgische MS Liga wenst te benadrukken dat elk oorzakelijk verband tussen Hepatitis B-vaccinatie en begin of deterioratie van MS ontbreekt (bevestiging november 2004).
Een dergelijke hypothetische relatie werd enkel in overweging genomen in Frankrijk, gezien het beleid van massieve vaccinatie, dat aldaar opgestart werd vanuit het ministerie van volksgezondheid. Sinds 1994 werden ongeveer 27 miljoen Fransen gevaccineerd tegen Hepatitis B, d.i. bijna de helft van de populatie. Deze verhouding stijgt tot bijna 66% in de leeftijdscategorie tussen 11 en 40 jaar. De andere Europese staten hebben een ander vaccinatiebeleid gevolgd, gericht op vaccinatie van jonge kinderen, preadolescenten (10-12 jaar) en volwassenen met verhoogd risico, nl. verhoogde kans op contact met bloed (medisch en paramedisch personeel).
In Frankrijk werd geen toename vastgesteld van de multiple sclerose frequentie aansluitend aan deze massieve vaccinatiecampagne. Geen enkele studie kon aantonen dat patiënten met beginnende multiple sclerose frequenter waren gevaccineerd dan patiënten uit dezelfde leeftijdscategorie consulterend voor een ander neurologisch probleem. Daaruit blijkt dat elke associatie tussen Hepatitis B-vaccinatie en het begin van multiple sclerose in de daaropvolgende weken als toevallig dient beschouwd.
Het Hepatitis-B virus is 100 maal meer besmettelijke dan het AIDS-virus. Het wordt in hoofdzaak overgedragen door contact met bloed van gezonde « dragers » of patiënten en tijdens seksueel contact. Desondanks blijft in 30% van de gevallen de overdrachtsvorm onbekend. Ongeveer één vierde van de gezonde dragers zullen ziek worden en overlijden aan levercirrhose of leverkanker in de 30 jaar volgend op de besmetting. Elk jaar overlijden 1 miljoen personen aan de gevolgen van Hepatitis B.
Wij adviseren dan ook een zelfde vaccinatie beleid aan te houden ten aanzien van patiënten met multiple sclerose en hun kinderen, als deze in de algemene Belgische bevolking nl. :
- Vaccinatie van jonge kinderen en preadolescenten
- Multiple Sclerose patiënten en hun volwassen kinderen, enkel vaccinatie bij personen met verhoogd risico (medisch & paramedisch personeel).
Caprivax (Goat serum) (februari 2004)
In de Britse media werd in oktober jl. een dubbelblind, placebogecontroleerde studie aangekondigd met een medicijn, Caprivax genaamd, dat blijkt te bestaan uit antistoffen afkomstig van het serum van geiten.
Aanvankelijk werd dit product ontwikkeld als een AIDS medicijn, doch het bleek niet erg actief te zijn. Omwille van ontstekingsremmende kenmerken, wordt het nu onderzocht bij MS. Het onderzoek gaat door bij personen met een secundair progressieve vorm van MS die nog kunnen stappen (cfr website MS liga UK).
In de wetenschappelijke publicaties zijn er op dit ogenblik geen gegevens beschikbaar over het product of de effecten hiervan bij MS . De vernoemde verantwoordelijke arts, D. Barnes, is momenteel telefonisch niet bereikbaar. Engelse MS experten zijn niet op de hoogte.
Vooraleer de beschreven positieve effecten bij personen met MS (Sunday Times, 25 januari 2004) ernstig te nemen, is verder onderzoek van deze gegevens nodig.
Inleiding
Steeds meer studies wijzen op een mogelijke bijdrage van de darmflora aan de gezondheid. Er zijn aanwijzingen dat de darmflora ook een rol zou kunnen spelen bij MS en andere chronische inflammatoire aandoeningen. De darmflora, een complex ecosysteem van bacteriën en andere micro-organismen, communiceert met het immuunsysteem en het centraal zenuwstelsel en is ook betrokken is bij de hormoonhuishouding en stofwisseling.
Hoe wordt de darmflora onderzocht?
De darmflora wordt onderzocht via een stoelgangstaal. Het genetisch materiaal van de micro-organismen wordt geïsoleerd en vervolgens ‘gelezen’ wat toelaat om de identiteit van de aanwezige micro-organismen te achterhalen en zo een darmflora profiel per persoon te kunnen samen stellen. Er zijn heel wat factoren (zoals medicatie, snellere/trage darmtransit, dieet, …) die de samenstelling van de darmflora kunnen beïnvloeden. Het is belangrijk om daarmee rekening te houden bij de interpretatie van de resultaten. Niet elke onderzoek neemt deze factoren mee. Ook zijn er nogal wat verschillen in de methodes om de stalen te bewaren en voor te bereiden.
Resultaten van het onderzoek
Momenteel is het niet mogelijk om vanuit het geheel aan onderzoeken naar de darmflora bij MS tot een eenduidige conclusie te komen.
Bij het onderzoek in België, een samenwerking tussen UZ/VU Brussel, KU Leuven en het Nationaal MS centrum Melsbroek, werden er verschillen gevonden in de kenmerken van de samenstelling van de darmflora tussen de verschillende vormen van ziekteverloop bij personen met MS. Daarnaast waren er enkele verschillen tussen MS als groep en de controlegroep. Aangezien de resultaten de weergave zijn van een doorsnede op één tijdspunt, is er momenteel geen uitspraak mogelijk over een oorzakelijk verband. Evenmin zijn er momenteel aanwijzingen om specifieke voedingsvoorschriften of bacteriële supplementen voor te schrijven. Wel pleiten deze resultaten voor verder onderzoek naar de rol van de darmflora bij MS. Wordt vervolgd!
Onderzoekers
MB D’hooghe (Center for Neurosciences, VU Brussel, Nationaal MS centrum Melsbroek)
L Devolder - T Reynders - A Pauwels (PhD onderzoekers)
J Raes (Moleculaire Bacteriologie, KU Leuven)
A Van Remoortel (studie coördinator, Nationaal MS centrum Melsbroek)
Link wetenschappelijk artikel https://pubmed.ncbi.nlm.nih.gov/32162850/
Prof. M.B. D’hooghe
Juni 2021
